
Pembahasan soal-soal Fisika Ujian Nasional (UN) tahun 2018 nomor 21 sampai dengan nomor 25 tentang:
- asas Black,
- laju perpindahan kalor,
- perpindahan kalor [sambungan logam],
- teori kinetik gas [tekanan gas],
- teori kinetik gas [kecepatan partikel gas].
Soal No. 21 tentang Asas Black
Air mendidih (100 ℃) sebanyak 250 ml dituangkan ke dalam panci berisi 400 ml air bersuhu 35 ℃. Setelah terjadi keseimbangan termal maka suhu campuran adalah … (kalor jenis air 1,0 kal.gr−1.℃−1).
A. 55 ℃
B. 60 ℃
C. 65 ℃
D. 75 ℃
E. 80 ℃
A. 55 ℃
B. 60 ℃
C. 65 ℃
D. 75 ℃
E. 80 ℃
Pembahasan
Air yang mendidih akan melepas kalor sedangkan air yang bersuhu 35 ℃ akan menyerap kalor. Keadaan ini dikenal sebagai asas Black yang dirumuskan:Qserap = Qlepas
mc(t − 35) = mc(100 − t)
400(t − 35) = 250(100 − t)
8(t − 35) = 5(100 − t)
8t − 280 = 500 - 5t
13t = 780
t = 780/13
= 60
Jadi, suhu campuran setelah terjadi keseimbangan termal adalah 60 ℃ (B).
Perdalam materi ini di Pembahasan Fisika UN: Kalor
Soal No. 22 tentang Laju Perpindahan Kalor
Besarnya kalor yang mengalir per detik melalui suatu bahan logam:
A. (1) dan (2)
B. (1) dan (3)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)
- berbanding terbalik dengan perbedaan suhu antara kedua ujungnya
- berbanding terbalik dengan luas penampang benda
- bergantung pada jenis bahan logam
- berbanding terbalik dengan panjang logam
A. (1) dan (2)
B. (1) dan (3)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)

Pembahasan
Besarnya kalor yang mengalir per detik melalui suatu bahan logam dirumuskan:
dengan:
H : kalor yang mengalir per detik (Q/t)
k : konduktivitas termal logam (bergantung jenis logam)
A : luas penampang logam
∆t : perbedaan suhu antarujung logam
l : panjang logam
Dengan demikian, besar kalor yang mengalir pada suatu logam:
- berbanding lurus dengan konduktivitas termal [pernyataan 3 benar]
- berbanding lurus dengan luas penampang logam [pernyataan 2 salah]
- berbanding lurus dengan perbedaan suhu kedua ujungnya [pernyataan 1 salah]
- berbanding terbalik dengan panjang logam [pernyataan 4 benar]
Perdalam materi ini di Pembahasan Fisika UN: Kalor
Soal No. 23 tentang Perpindahan Kalor [sambungan logam]
Logam P, Q, dan R berukuran sama. Konduktivitas logam P, Q, dan R berturut-turut adalah 4k, 2k, dan k. Ketiganya terhubung dengan suhu pada ujung-ujung terbuka seperti pada gambar berikut.

Suhu pada sambungan logam P dengan Q (Tx) adalah ….
A. 80 ℃
B. 70 ℃
C. 60 ℃
D. 50 ℃
E. 40 ℃

Suhu pada sambungan logam P dengan Q (Tx) adalah ….
A. 80 ℃
B. 70 ℃
C. 60 ℃
D. 50 ℃
E. 40 ℃
Pembahasan
Rumus yang digunakan untuk menyelesaikan soal di atas sama dengan rumus pada soal no. 22.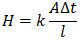
Karena ketiga logam tersebut berukuran sama (A dan l sama), kalor yang diserap/dilepas hanya sebanding dengan k dan ∆t.
H ~ k∆t
Pada sambungan P-Q, kalor yang dilepas Q akan diserap P.
kP (Tx − 20) = kQ (Ty − Tx)
4k(Tx − 20) = 2k(Ty − Tx)
2(Tx − 20) = Ty − Tx
2Tx − 40 = Ty − Tx
3Tx = Ty + 40
Ty = 3Tx − 40 … (1)
Sedangkan pada sambungan Q-R, kalor yang dilepas R akan diserap Q.
kQ (Ty − Tx) = kR (160 − Ty)
2k(Ty − Tx) = k(160 − Ty)
2(Ty − Tx) = 160 − Ty
2Ty − 2Tx = 160 − Ty
3Ty = 2Tx + 160 … (2).
Selanjutnya kita substitusikan persamaan (1) ke persamaan (2).
3(3Tx − 40) = 2Tx + 160
9Tx − 120 = 2Tx + 160
7Tx = 280
Tx = 40
Jadi, suhu pada sambungan logam P dengan Q (Tx) adalah 40 ℃ (E).
Perdalam materi ini di Pembahasan Fisika UN: Kalor
Soal No. 24 tentang Teori Kinetik Gas [tekanan gas]
Perhatikan pernyataan berikut!
A. (1), (2), (3), dan (4)
B. (1), (2), dan (3)
C. (1) dan (3)
D. (2) dan (4)
E. (3) dan (4)
- Jumlah partikel gas ditambah
- Jumlah mol dikurangi
- Suhu ditingkatkan
- Volume ditambah
A. (1), (2), (3), dan (4)
B. (1), (2), dan (3)
C. (1) dan (3)
D. (2) dan (4)
E. (3) dan (4)
Pembahasan
Untuk menjawab soal di atas, kita gunakan persamaan umum gas ideal:PV = nRT → P = nRT/V
PV = NkT → P = NkT/V
Berdasarkan kedua rumus di atas dapat disimpulkan bahwa tekanan gas (P):
- berbanding lurus dengan jumlah mol (n), jumlah partikel (N), dan suhu (T)
- berbanding terbalik dengan volume (V).
- jumlah mol ditambah [no. 2 salah]
- jumlah partikel ditambah [no. 1 benar]
- suhu dinaikkan [no. 3 benar]
- volume dikurangi [no. 4 salah]
Perdalam materi ini di Pembahasan Fisika UN: Teori Kinetik Gas
Soal No. 25 tentang Teori Kinetik Gas [kecepatan partikel gas]
Gas argon berada dalam ruangan tertutup saat suhunya berubah menjadi dua kali semula maka kecepatan gerak partikel gas argon adalah ….
A. 1/2 kali semula
B. 1/√2 kali semula
C. √2 kali semula
D. 2 kali semula
E. 4 kali semula
A. 1/2 kali semula
B. 1/√2 kali semula
C. √2 kali semula
D. 2 kali semula
E. 4 kali semula
Pembahasan
Diketahui:T2 = 2T1
Hubungan antara kecepatan gerak partikel dan suhu dapat dirunut dari rumus:
Ek = 3/2 kT
1/2 mv2 = 3/2 kT
Sehingga hubungan antara keduanya adalah:

Jadi, kecepatan gerak partikel gas argon adalah √2 kali semula (C).
Perdalam materi ini di Pembahasan Fisika UN: Teori Kinetik Gas
Simak Pembahasan Soal Fisika UN 2018 selengkapnya.
| No. 01 - 05 | No. 21 - 25 | ||||
| No. 06 - 10 | No. 26 - 30 | ||||
| No. 11 - 15 | No. 31 - 35 | ||||
| No. 16 - 20 | No. 36 - 40 |
Dapatkan pembahasan soal dalam file pdf di sini.
Demikian, berbagi pengetahuan bersama Kak Ajaz. Silakan bertanya di kolom komentar apabila ada pembahasan yang kurang jelas. Semoga berkah.

No. 25 kok langsung ada rumus 3/2 kT dari mana ya?
ReplyDeleteSaya waktu sekolah dulu, rumus itu saya hafalkan. Jika tidak, maka harus diturunkan dari rumus asalnya sbb:
Deletep = 1/3 (Nmv^2)/V
karena Ek = 1/2 mv^2 maka mv^2 = 2 Ek
sehingga rumus di atas menjadi
p = 1/3 N/V 2 Ek
atau
pV = 2/3 N Ek
Sementara itu pV = NkT sehingga
NkT = 2/3 N Ek
atau
Ek = 3/2 kT