Pembahasan soal Kimia Ujian Nasional (UN) tahun 2018 nomor 31 sampai dengan nomor 35 tentang:
- isomer senyawa karbon,
- sifat senyawa karbon,
- polimer,
- stoikiometri, dan
- karbohidrat.
Soal No. 31 tentang Isomer Senyawa Karbon
Berikut ini adalah pasangan senyawa karbon.
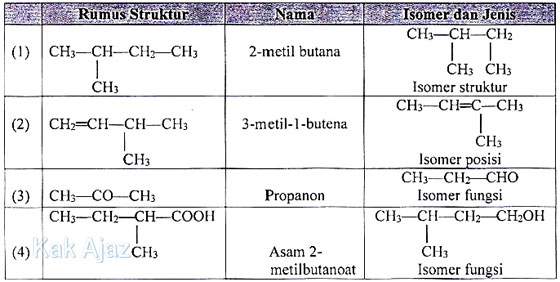
Pasangan senyawa karbon yang benar adalah ….
A. (1) dan (2)
B. (1) dan (3)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)

Pasangan senyawa karbon yang benar adalah ….
A. (1) dan (2)
B. (1) dan (3)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)
Pembahasan
Jika kita amati tabel di atas, antara rumus struktur dan nama senyawa adalah benar. Sehingga kita cukup menentukan apakah isomernya benar atau tidak.Mari kita periksa satu per satu!
- Bukan isomer, hanya beda gambar saja. Rantai panjang yang pertama digambar lurus, sedangkan yang kedua digambar berbelok sehingga namanya tetap sama. [salah]
- Isomer posisi, beda letak ikatan rangkap. Nama yang pertama 3-metil-1-butena, yang kedua 2-metil-2-butena. [benar]
- Isomer fungsi, beda gugus fungsi. Nama yang pertama propanon (golongan alkanon), yang kedua propanal (golongan aldehid). [benar]
- Bukan isomer. Yang pertama golongan asam karboksilat dengan nama asam 2-metilbutanoat sedangkan yang kedua golongan alkohol dengan nama 3-metilbutanol. Asam karboksilat dan alkohol tidak berisomer fungsi. [salah]
Perdalam materi ini di Pembahasan Kimia UN: Senyawa Karbon
Soal No. 32 tentang Sifat Senyawa Karbon
Perhatikan rumus struktur senyawa C3H6O berikut ini!
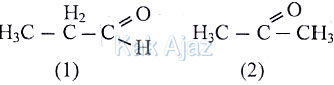
Perbedaan sifat kimia senyawa (1) dan senyawa (2) yang tepat adalah ….
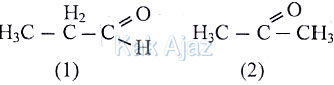
Perbedaan sifat kimia senyawa (1) dan senyawa (2) yang tepat adalah ….
| Senyawa (1) | Senyawa (2) | |
| A. | Dapat direduksi menjadi senyawa yang bereaksi dengan natrium | Dapat direduksi menjadi senyawa yang tidak bereaksi dengan logam natrium |
| B. | Dapat dioksidasi menjadi alkohol primer | Dapat dioksidasi menjadi alkohol sekunder |
| C. | Dapat diidentifikasi dengan pereaksi tollens menghasilkan cermin perak | Tidak dapat bereaksi dengan pereaksi tollens |
| D. | Dapat dioksidasi menghasilkan senyawa yang dapat memerahkan lakmus biru | Tidak dapat dioksidasi menjadi senyawa organik lainnya |
| E. | Dapat bereaksi dengan logam natrium | Tidak dapat bereaksi dengan logam natrium |

Pembahasan
Senyawa (1) adalah propanal (golongan aldehid) sedangkan senyawa (2) adalah propanon (golongan keton.Di antara sifat-sifat kimia aldehid dan keton adalah sebagai berikut:
- Aldehid dapat direduksi menjadi alkohol primer sedangkan keton dapat direduksi menjadi alkohol sekunder. Semua alkohol dapat bereaksi dengan logam natrium menjadi natrium alkoholat. [opsi A salah]
- Aldehid dapat dioksidasi menjadi asam karboksilat sedangkan keton tidak dapat dioksidasi. [opsi B salah, opsi D benar]
- Aldehid dapat diidentifikasi dengan pereaksi Fehling menghasilkan endapan merah bata dan dengan pereaksi Tollens menghasilkan endapan cermin perak. Sedangkan keton tidak bereaksi dengan pereaksi Fehling maupun Tollens. [opsi C benar]
Perdalam materi ini di Pembahasan Kimia UN: Senyawa Karbon
Soal No. 33 tentang Polimer
Polimer yang terbentuk jika 2 jenis monomer berikut ini

bereaksi adalah ….
A. Bakelit
B. Dakron
C. Nilon 66
D. Perspex
E. Polistirena

bereaksi adalah ….
A. Bakelit
B. Dakron
C. Nilon 66
D. Perspex
E. Polistirena
Pembahasan
Berikut ini tabel polimer dan monomer pembentuknya.| Polimer | Monomer |
| Bakelit | - fenol - metanal |
| Poliester (dakron) | - asam tereftalat - etanadiol |
| Poliamida (nilon 66) | - asam adipat (heksanadiol diklorida) - 1,6-diaminoheksana |
| Perspex | metilmetaklirat |
| Polistirena | vinil etena |
Jadi, polimer yang terbentuk dari 2 jenis monomer tersebut adalah nilon 66 (C).
Perdalam materi ini di Pembahasan Kimia UN: Polimer
Soal No. 34 tentang Stoikiometri
Pembakaran sempurna gas etanol sebagai bahan bakar alternatif mengikuti persamaan berikut.
C2H5OH(g) + O2(g) → CO2(g) + H2O(g) [belum setara]
Jika pada pembakaran tersebut dibutuhkan 5,6 L dan volume etanol yang dibakar 1,12 L, massa air yang terbentuk diukur pada keadaan STP adalah … (Mr H2O = 18 L)
A. 1,8 g
B. 2,7 g
C. 9,0 g
D. 18 g
E. 27 g
C2H5OH(g) + O2(g) → CO2(g) + H2O(g) [belum setara]
Jika pada pembakaran tersebut dibutuhkan 5,6 L dan volume etanol yang dibakar 1,12 L, massa air yang terbentuk diukur pada keadaan STP adalah … (Mr H2O = 18 L)
A. 1,8 g
B. 2,7 g
C. 9,0 g
D. 18 g
E. 27 g
Pembahasan
Reaksi setara untuk reaksi di atas adalah:C2H5OH + 3O2 → 2CO2 + 3H2O
Karena diukur pada keadaan STP maka:
mol C2H5OH = 1,12/22,4
= 0,05
Sedangkan mol H2O dapat dicari berdasarkan perbandingan koefisien:
mol H2O = 3/1 × mol C2H5H
= 3 × 0,05
= 0,15
Dengan demikian, massa H2O adalah:
gr H2O = mol × Mr
= 0,15 × 18
= 2,7
Jadi, massa air yang terbentuk adalah 2,7 g (B).
Perdalam materi ini di Pembahasan Kimia UN: Stoikiometri
Soal No. 35 tentang Karbohidrat
Untuk menentukan kadar gula dalam tubuh pasien digunakan pereaksi ….
A. Fehling, karena pereaksi ini lebih spesifik untuk mengidentifikasi gugus aldehid
B. Molisch, karena pereaksi ini dapat mengidentifikasi zat golongan karbohidrat
C. Millon, karena pereaksi ini dapat menentukan adanya fenol dalam protein
D. Ninhidrin, karena pereaksi ini dapat mendeteksi asam amino
E. Seliwanoff, karena pereaksi ini dapat membedakan gula aldosa dan ketosa
A. Fehling, karena pereaksi ini lebih spesifik untuk mengidentifikasi gugus aldehid
B. Molisch, karena pereaksi ini dapat mengidentifikasi zat golongan karbohidrat
C. Millon, karena pereaksi ini dapat menentukan adanya fenol dalam protein
D. Ninhidrin, karena pereaksi ini dapat mendeteksi asam amino
E. Seliwanoff, karena pereaksi ini dapat membedakan gula aldosa dan ketosa
Pembahasan
Kadar gula adalah kandungan glukosa dalam tubuh kita. Glukosa merupakan gula pereduksi atau gula yang mengandung gugus aldehid. Sehingga untuk mengidentifikasinya digunakan pereaksi Fehling atau Benedict.Jadi, untuk menentukan kadar gula dalam tubuh pasien digunakan pereaksi Fehling (A).
Perdalam materi ini di Pembahasan Kimia UN: Karbohidrat dan Protein
Simak Pembahasan Soal Kimia UN 2018 selengkapnya.
| No. 01 - 05 | No. 21 - 25 | ||||
| No. 06 - 10 | No. 26 - 30 | ||||
| No. 11 - 15 | No. 31 - 35 | ||||
| No. 16 - 20 | No. 36 - 40 |
Dapatkan pembahasan soal dalam file pdf di sini.
Demikian, berbagi pengetahuan bersama Kak Ajaz. Silakan bertanya di kolom komentar apabila ada pembahasan yang kurang jelas. Semoga berkah.

makasih banget ka, sangat berfanfaat
ReplyDeleteSama-sama. Semoga berkah
Deletemakasi kaak :))
ReplyDeleteMakasih kembali. Semoga bermanfaat
DeleteTerima kasih,
ReplyDeleteAda ngk soal UNBK
Sama-sama. Semoga bermaanfaat.
DeleteUNBK yang full 1 paket tidak punya, hanya soal-soal tertentu saja. Itu pun mirip dengan soal UNKP